EVALUACIÓN DE PERIODO
viernes, 31 de mayo de 2019
Semana 18
Quiz
Primera clase : se hace repaso y luego se realiza quiz ( a partir del nombre hacer la estructura).
Segunda clase: Se hace repaso y luego se realiza quiz( a partir de la estructura hacer el nombre )
Primera clase : se hace repaso y luego se realiza quiz ( a partir del nombre hacer la estructura).
Segunda clase: Se hace repaso y luego se realiza quiz( a partir de la estructura hacer el nombre )
Semana 17
clase 1 :
Se realiza la celebración del dia del Maestro y se pierde la clase.
clase 2:
No se realiza la clase ya que se desarolla la inaguración del torneo interclases.
Se realiza la celebración del dia del Maestro y se pierde la clase.
No se realiza la clase ya que se desarolla la inaguración del torneo interclases.
Semana 15
Contituación de los ejemplos del Documento
5-etil-4,6dimetil/oct/a-4-en-2,7-diino-1,6-ditiol
H CH3
| |
HS - C - C - C -C - C- C-C-C-H
| | |
CH3 CH2 SH
|
CH3
raiz: oct prefijo 1:lineal prefijo 2: 5 etil-4,6-dimetil sufijo 1:4-en-2,7-diino sufijo 2: 1,6 -ditiol



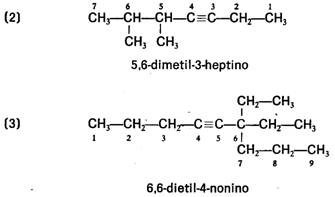
5-etil-4,6dimetil/oct/a-4-en-2,7-diino-1,6-ditiol
H CH3
| |
HS - C - C - C -C - C- C-C-C-H
| | |
CH3 CH2 SH
|
CH3
raiz: oct prefijo 1:lineal prefijo 2: 5 etil-4,6-dimetil sufijo 1:4-en-2,7-diino sufijo 2: 1,6 -ditiol




Semana 14
EJERCICIOS DEL NOMBRE A LA ESTRUCTURA
° Acido- 4- metil-2-ceto-3,3 di ( 1-metil/etenil)-4-pentenoico


° Acido- 4- metil-2-ceto-3,3 di ( 1-metil/etenil)-4-pentenoico
raiz:pent
sufijo:en
C--CH2
|
C -- C - C - C - C =O
| | || |
CH3 C O OH
| - CH2
CH3


° 3,7- dietril-4,8-dimetil-5-(1,1,2 -trimetril/prop/il)- 2,5- non/adieno
H H H H H
| | | | |
H3C - CH2 - C - C -C - C - C - C - CH3
| | | | | |
CH2 CH3 C H CH2 CH3
Semana 13
Ejemplos de la nomenclatura de hidrocarburos
Ejemplo 1
O O
|| ||
C - CH2 - CH - CH2 - CH2 - C - OH
|
OH
Raíz: hex
Sufijo 1°: an
Sufijo 2°: 1,6-dioico
Prefijo 2°: hidroxi
Ejemplo 2
1 2 3 4 5 6 7
CH3 - C - CH2- CH- C- CH2- CH3
|| | ||
O OH O
2,5-diona
4-hidroxi 4-hidroxi-2,5- heptanodiona
raiz:hept
suf. 1° : an - sencillo
suf.2° : 2,5 - diona
prefijo 1 ° : lineal
prefijo 2° : 4- hidroxi
Aromaticidad
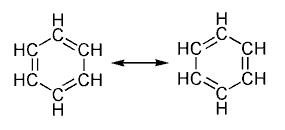
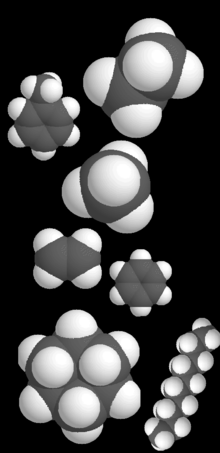
Eso quiere decir que al representar la molécula se dibujan los enlaces dobles en una configuración y, entre flechas, las demás configuraciones como oportunidades adicionales tengan los electrones de los enlaces dobles de formar otros enlaces alrededor del anillo aromático. La molécula de benceno, por ejemplo tiene varios estados de resonancia, de los cuales dos son representados aquí, que corresponden a los enlaces dobles alternándose con los enlaces simples.
Enlaces dobles del benceno
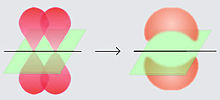
Dos orbitales p formando un enlace π.
Eso quiere decir que en vez de estar comprometidos a un solo átomo de carbono, cada electrón (de cada doble enlace original) es compartido por los seis átomos de carbono en el benceno:
Semana 12
NOMENCLATURA DE LOS HIDROCARBUROS
Para nombrar los hidrocarburos hay que tener encuenta el prefijo-Raiz-Sufijo
:Raíz :Esta constituye el numero de carbonos de la cadena principal .
Prefijos :
| Prefijos griegos | Número de átomos |
| mono- | 1 |
| di- | 2 |
| tri- | 3 |
| tetra- | 4 |
| penta- | 5 |
| hexa- | 6 |
| hepta- | 7 |
| octa- | 8 |
| non-, nona-, eneá- | 9 |
| deca- | 10 |
Sufijo secundario : Están ordenados,según lo establecido convencionalmente por la I.U.P.A.C , en orden decreciente de importancia .
Cadena principal o raíz :
Es a secuencia carbonada progenitora del compuesto particular y
equivale al hidrocarburo no ramificado del mismo numero de atomos de
carbono.
GRUPOS FUNCIONALES QUE CONTIENEN OXÍGENO
Alcoholes
Los alcoholes poseen un enlace C-O-H,
es decir, se tiene un oxígeno unido tanto a un carbono como a un
hidrógeno por medio de enlaces simples. En forma abreviada, lo
representamos así:
Los
alcoholes que no tienen muchos átomos de carbono son solubles en agua
y, por lo general, son líquidos a temperatura ambiente (o tienen un
punto de ebullición relativamente alto). Esto se debe a que son capaces
de formar enlaces de hidrógeno.
El etanol C2H5OH
es uno de los alcoholes más conocidos por nosotros. Lo usamos como
desinfectante y es el componente principal de las bebidas alcohólicas.
Otro alcohol es el mentol, presente en el aceite de menta, usado en cremas dentales por su olor y sabor característico.
Éteres
Los éteres poseen un oxígeno unido a dos átomos de carbono por medio de enlaces simples. En general:
Los
éteres tienen punto de ebullición menor que los alcoholes, puesto que
no presentan fuerzas intermoleculares de enlace de hidrógeno. Asimismo,
debido a esto, son muy poco solubles en agua.
El éter etílico es muy conocido como solvente y fue usado durante muchos años como anestésico, debido a su peculiar olor (que da sueño). El anisol, por otro lado, es el responsable del olor del anís.
Aldehídos y cetonas
Los aldehídos y cetonas presentan un doble enlace entre un carbono y un oxígeno (denominado grupo carbonilo). La diferencia entre ellos radica en los átomos adyacentes al carbono en mención. En general:
Observa las semejanzas y diferencias entre un aldehído y una cetona: ambos tienen un grupo carbonilo (C=O).
El aldehído tiene, unido al carbono del carbonilo, un carbono y un
hidrógeno, mientras que una cetona tiene unido sólo átomos de carbono.
Los
aldehídos y cetonas con pocos átomos de carbono son solubles en agua.
Por lo general son líquidos a temperatura ambiente, aunque tienen bajo
punto de ebullición.
El cinamaldehído es un aldehído que se encuentra en la canela y es responsable del olor. La acetona es la cetona más simple, y se usa como disolvente (por ejemplo, para quitar el esmalte de uñas).
Ácidos carboxílicos
Los ácidos carboxílicos poseen también un grupo carbonilo, pero el carbono está unido, también, a un grupo OH. En general:
- Si poseen un radical se toma el nombre del ciclo como la cadena principal:
 |  |  |
| Etilciclopentano | Metilciclobutano | Propilciclohexeno |
La
secuencia principal debe ser la cadena continua mas extensa de
átomos de carbono que cumple el siguiente orden de prioridades ,
incluyendo :
| Nombre | Radical | ||||
| metil | - CH3 | ||||
| etil | - CH2 - CH3 | ||||
| propil | - CH2 - CH2 - CH3 | , |
4.- Como los radicales pueden ir colocados en distintos carbonos, debemos indicar en qué carbono están colocados. Para ello numeramos la cadena y, al nombrar el radical, anteponemos un número que indica en que carbono de la cadena principal está colocado.

La cadena principal es la enmarcada en rojo. Luego sería 5 metil hexano, si empiezo a contar por la derecha o 2 metil hexano, si empiezo por la izquierda. La norma dice que hay que empezar por el lado tal que los números de los radicales sean los más bajos. Por eso, sería 2 metil hexano.
5.- Cuando la cadena lleva dobles o triples enlaces, también debemos indicar en que carbono va ese doble o triple enlace, significándolo con un número que indica el carbono anterior a ese enlace. Se aplica la misma norma de numeración, de forma que caigan las insaturaciones (dobles y triples enlaces) con el número más bajo. Las insaturaciones tienen preferencia a la hora de numerar sobre los radicales.

Este sería el 5 metil 2 hexeno, pues se numera por la izquierda, para que el doble enlace caiga con el
número más bajo.
Semana 11
Los Hidrocarburos
Los hidrocarburos son compuestos orgánicos formados únicamente por átomos de carbono e hidrógeno. Son los compuestos básicos que estudia la química orgánica.Las cadenas de átomos de carbono pueden ser lineales o ramificadas, y abiertas o cerradas. Los que tienen en su molécula otros elementos químicos (heteroátomos) se llaman hidrocarburos sustituidos.
La mayoría de los hidrocarburos que se encuentran en nuestro planeta ocurren naturalmente en el petróleo crudo, donde la materia orgánica descompuesta proporcionó una abundancia de carbono e hidrógeno, los que pudieron catenarse para formar cadenas aparentemente ilimitadas. Los hidrocarburos pueden encontrarse también en algunos planetas sin necesidad de que haya habido vida para generar petróleo, como en Júpiter, Saturno, Titán y Neptuno, compuestos parcialmente por hidrocarburos como el metano o el etano.
Clasificación
Hidrocarburos saturados o alcanos: son compuestos formados por carbono e hidrógeno, presentan enlaces sencillos (SP3). Presenta una fórmula general (CnH2n+2), donde n es el número de carbonos del compuesto y el sufijo o y su terminación es ano.
CH4→ Metano, C2H6→Etano, C3H8→Propano,
C4H10→Butano, C5H12→Pentano, C6H14→ Hexano,
C7H16→Heptano
C8H18→Octano, C9H20→Nonano, C10H22→Decano.
De acuerdo al tipo de estructuras que pueden formar, los hidrocarburos se pueden clasificar en:
- Hidrocarburos acíclicos, los cuales presentan sus cadenas abiertas. A su vez se clasifican en:
- Hidrocarburos lineales a los que carecen de cadenas laterales
- Hidrocarburos ramificados, los cuales presentan cadenas laterales.
- Hidrocarburos cíclicos o cicloalcanos, que se definen como hidrocarburos de cadena cerrada. Estos a su vez se clasifican como:
- Monocíclicos, que tienen una sola operación de ciclización.
- Policíclicos, que contienen varias operaciones de ciclización.
Suscribirse a:
Entradas (Atom)