Ejemplos de la nomenclatura de hidrocarburos
Ejemplo 1
O O
|| ||
C - CH2 - CH - CH2 - CH2 - C - OH
|
OH
Raíz: hex
Sufijo 1°: an
Sufijo 2°: 1,6-dioico
Prefijo 2°: hidroxi
Ejemplo 2
1 2 3 4 5 6 7
CH3 - C - CH2- CH- C- CH2- CH3
|| | ||
O OH O
2,5-diona
4-hidroxi 4-hidroxi-2,5- heptanodiona
raiz:hept
suf. 1° : an - sencillo
suf.2° : 2,5 - diona
prefijo 1 ° : lineal
prefijo 2° : 4- hidroxi
Aromaticidad
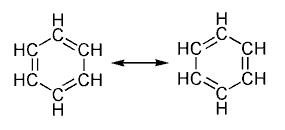
Eso quiere decir que al representar la molécula se dibujan los enlaces dobles en una configuración y, entre flechas, las demás configuraciones como oportunidades adicionales tengan los electrones de los enlaces dobles de formar otros enlaces alrededor del anillo aromático. La molécula de benceno, por ejemplo tiene varios estados de resonancia, de los cuales dos son representados aquí, que corresponden a los enlaces dobles alternándose con los enlaces simples.
Enlaces dobles del benceno
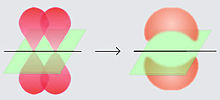
Dos orbitales p formando un enlace π.
Eso quiere decir que en vez de estar comprometidos a un solo átomo de carbono, cada electrón (de cada doble enlace original) es compartido por los seis átomos de carbono en el benceno:
No hay comentarios.:
Publicar un comentario